Renne (Rangifer tarandus)
Le renne (Rangifer tarandus) est un mammifère emblématique des régions arctiques et subarctiques. Il se distingue par son adaptation remarquable aux environnements froids, notamment grâce à son pelage isolant et ses larges sabots. Contrairement aux autres cervidés, le renne est le seul dont les deux sexes portent des bois, bien que ceux de la femelle soient généralement plus petits. Cet herbivore grégaire est célèbre pour ses vastes migrations saisonnières à travers la toundra et la taïga, parcourant souvent des milliers de kilomètres. Il joue un rôle écologique crucial dans la régulation de la végétation et constitue une ressource vitale pour les peuples autochtones. Sa large distribution et ses variations morphologiques ont mené à la reconnaissance de nombreuses sous-espèces, reflétant une histoire évolutive complexe face aux cycles glaciaires et interglaciaires. Le renne est également appelé Caribou en Amérique du Nord.

© Manimalworld
 CC-BY-NC-SA (Certains droits réservés)
CC-BY-NC-SA (Certains droits réservés)Le renne présente une morphologie robuste et compacte, parfaitement adaptée à la rigueur des climats froids. Les adultes affichent une hauteur au garrot variant généralement entre 1 et 1,5 mètre et un poids qui peut atteindre 180 à 270 kg pour les mâles les plus imposants, tandis que les femelles sont plus légères. La tête est proportionnellement longue et porte des bois ramifiés qui, fait unique chez les cervidés, sont présents chez les mâles et chez les femelles. La forme et la taille des bois varient grandement, avec des pointes souvent aplaties appelées "palettes".
Le corps est recouvert d'un pelage exceptionnellement dense et isolant, dont la couleur varie du brun foncé au gris-blanc selon la saison et la sous-espèce. Ce pelage est composé de deux couches : un sous-poil laineux et des poils de garde longs et creux, remplis d'air, offrant une isolation thermique remarquable et une flottabilité accrue lors de la traversée de cours d'eau.
Les pattes, relativement courtes, se terminent par des sabots larges et concaves qui s'écartent en éventail. Cette caractéristique est essentielle pour la marche sur la neige ou les sols mous et permet de creuser pour atteindre la nourriture sous la neige. De plus, un tendon dans le pied émet un cliquetis audible lors de la marche, un son distinctif produit par le claquement de l'os sésamoïde.

© Manimalworld
 CC-BY-NC-SA (Certains droits réservés)
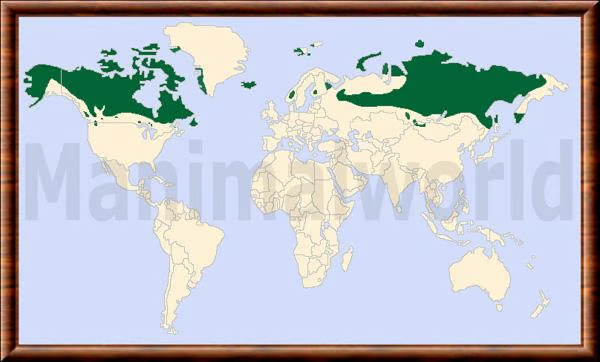
CC-BY-NC-SA (Certains droits réservés)Le renne est largement distribué dans l'Arctique et le subarctique, s'étendant de 50 à 81 degrés de latitude. Son aire de répartition naturelle englobe le nord-ouest des États-Unis, l'Alaska, le Canada, le Groenland, la Norvège, la Finlande, la Russie et la Mongolie. Historiquement, cette distribution a été modifiée par l'introduction de rennes domestiques, dont certains se sont ensauvagés, notamment en Islande et sur plusieurs îles de l'Atlantique Sud (Kerguelen, Malouines).
Cependant, au cours du siècle dernier, l'aire de répartition géographique de l'espèce s'est considérablement contractée et fragmentée. Ce déclin est principalement attribué à la chasse et aux altérations du paysage induites par l'accroissement des établissements humains, l'agriculture, la foresterie, et le développement de l'élevage. Des analyses nationales témoignent de ce phénomène. Le renne des forêts a disparu de Finlande au début des années 1900 avant qu'une petite zone ne soit recolonisée depuis la Russie. En Norvège, l'aire de répartition cumulée a diminué de moitié, tandis qu'en Russie, la distribution s'est contractée vers le nord et l'ouest, entraînant une fragmentation sur plus de 85 % de son territoire.
Au Canada, le caribou boréal a perdu environ la moitié de son ancienne aire de répartition au cours des 150 dernières années, avec des pertes atteignant 60 % en Alberta et 50 % en Ontario. La population du caribou de la Gaspésie-Atlantique, autrefois plus étendue, est désormais un simple vestige. Par ailleurs, l'aire de répartition annuelle du caribou des montagnes en Colombie-Britannique a diminué de 40 % en 2002. Bien que l'évolution de la répartition du caribou de la toundra soit compliquée par ses cycles d'abondance naturels, des déclins historiques, comme celui du troupeau de Fortymile en Alaska, ont également entraîné une réduction de 25 % de l'aire.
Cette situation est préoccupante, car une documentation insuffisante sur la répartition historique fait que la distribution actuelle et réduite pourrait être perçue comme la norme, un phénomène connu sous le nom de "changement de référence".
© Manimalworld
 CC-BY-NC-SA (Certains droits réservés)
CC-BY-NC-SA (Certains droits réservés)L'alimentation du renne est principalement herbivore et opportuniste, s'adaptant étroitement aux ressources disponibles dans les écosystèmes arctiques et subarctiques. Durant les mois d'été, lorsque la végétation est abondante et diversifiée, son régime alimentaire est composé de feuilles d'arbres nains, de graminées, de carex, de fleurs et de pousses d'arbustes comme le saule et le bouleau. Ces aliments fournissent les nutriments et l'énergie nécessaires pour accumuler des réserves de graisse cruciales en vue de l'hiver et de la période de reproduction.
Cependant, l'élément le plus distinctif de son régime, particulièrement en hiver, est le lichen, souvent appelé "mousse de renne" (Cladonia rangiferina). Malgré sa faible teneur en protéines, le lichen est riche en glucides digestibles et constitue une source d'énergie vitale lorsque le sol est couvert de neige. Les rennes sont dotés de capacités remarquables pour localiser le lichen sous une épaisse couche de neige grâce à leur odorat très développé, creusant la neige avec leurs sabots. Leur système digestif est spécialement adapté pour métaboliser efficacement cette nourriture fibreuse. En outre, il a été observé que les rennes peuvent boire de l'eau salée ou de manger de la neige riche en minéraux pour satisfaire leurs besoins en sel et en oligo-éléments, illustrant leur flexibilité alimentaire en milieu hostile.

Crédit photo: Alex Kantorovich - Zooinstitutes
La reproduction du renne est un événement saisonnier fortement synchronisé, commençant par le rut qui se déroule généralement à l'automne, de fin septembre à novembre, après les grandes migrations estivales. Les mâles développent une épaisse crinière et perdent une quantité importante de graisse corporelle en se livrant à des combats spectaculaires pour l'accès aux femelles, utilisant leurs bois comme armes. Ces luttes de dominance déterminent quels mâles auront le droit de s'accoupler avec les femelles, formant ainsi des harems qui peuvent compter jusqu'à 15 ou 20 individus. Le mâle dominant défend farouchement son harem, ce qui explique son épuisement physique à la fin de la saison de reproduction.
La gestation dure en moyenne environ 7,5 mois (227 à 247 jours), permettant la mise bas de la plupart des faons (un seul par femelle) au printemps, généralement en mai ou début juin. Cette période coïncide avec l'arrivée de la végétation nouvelle et plus nutritive, essentielle pour la survie du nouveau-né. Le faon, extrêmement précoce, est capable de se tenir debout et de courir quelques heures seulement après la naissance, une adaptation cruciale pour suivre la harde et échapper aux prédateurs dans leur environnement ouvert. La mère et son petit développent un lien fort et le faon est sevré au cours de l'été, bien qu'il puisse rester avec sa mère jusqu'à la saison de reproduction suivante. L'atteinte de la maturité sexuelle varie, intervenant généralement vers l'âge de 1,5 à 3 ans pour les femelles, et plus tardivement pour les mâles qui doivent acquérir une taille et une force suffisantes pour concurrencer les adultes.
La longévité du renne varie selon les conditions environnementales, la pression des prédateurs et le statut sauvage ou domestique. En milieu naturel, les rennes vivent en moyenne entre 10 et 15 ans, bien que certains individus puissent atteindre 18 ans dans des zones où les prédateurs sont rares et la nourriture abondante. Les populations domestiquées, mieux protégées et nourries, peuvent parfois dépasser 20 ans. La mortalité juvénile est élevée, surtout durant les premiers mois de vie, période critique où les faons sont particulièrement vulnérables au froid, à la famine et aux attaques.

© Johnal Palahniuk - iNaturalist
 CC-BY-NC (Certains droits réservés)
CC-BY-NC (Certains droits réservés)Le comportement du renne est fortement dominé par sa nature grégaire et ses migrations saisonnières, considérées comme parmi les plus longues et les plus massives de tous les mammifères terrestres.
Les rennes vivent en hardes de taille variable, allant de petits groupes familiaux en hiver à d'immenses rassemblements pouvant compter des dizaines de milliers d'individus pendant les migrations estivales. Ces mouvements de masse sont principalement motivés par la recherche de pâturages saisonniers, la fuite des parasites (mouches, moustiques) en été et le déplacement vers des zones de mise bas sécurisées et riches en nourriture printanière. L'organisation sociale au sein de la harde est relativement souple mais basée sur l'expérience et la dominance. Pendant la migration, les femelles gravides et les faons se positionnent souvent en tête, tandis que les mâles et les juvéniles suivent.
La communication s'effectue par des vocalisations (grognements, soufflements), des signaux visuels (postures, mouvements des bois) et des signaux chimiques (phéromones), jouant un rôle vital dans la cohésion du groupe et l'établissement des hiérarchies. En plus du cratérage pour trouver leur nourriture hivernale, les rennes font preuve d'une vigilance constante face aux prédateurs. Leur excellente ouïe et leur odorat très fin, couplés à leur vitesse et leur endurance, sont leurs principaux atouts pour survivre dans les vastes étendues arctiques. Cette dynamique de groupe offre une protection collective contre les menaces et optimise l'accès aux ressources dans un environnement parfois très dispersé.

© Klaus Rudloff - BioLib
 All rights reserved (Tous droits réservés)
All rights reserved (Tous droits réservés)Malgré leur grande taille et leur nature grégaire, les rennes sont la proie de plusieurs prédateurs naturels, surtout dans les zones de toundra ouverte où ils sont particulièrement vulnérables. Le prédateur le plus significatif et redouté est le loup gris (Canis lupus). Les loups chassent souvent en meute, ciblant généralement les individus faibles, malades, vieux ou très jeunes, en particulier les faons nés au printemps. Les rennes se défendent en courant ou en donnant de violents coups de sabots. La stratégie de défense la plus efficace contre les loups est la fuite coordonnée au sein de la harde, se déplaçant en formation serrée pour minimiser les opportunités d'attaque.
Un autre prédateur important, bien que chassant souvent en solitaire, est le grizzly (Ursus arctos horribilis), particulièrement actif après l'hibernation pour reconstruire ses réserves de graisse. Les ours bruns s'attaquent principalement aux faons, aux femelles en mauvaise condition ou peuvent parfois s'approprier les carcasses de rennes tués par les loups. Dans le Grand Nord canadien et au Groenland, le Caribou de Peary et d'autres sous-espèces sont également la proie du renard polaire (Vulpes lagopus) et du carcajou (Gulo gulo) qui s'attaquent surtout aux jeunes.
L'impact de la prédation varie en fonction des conditions environnementales et de la taille des populations des deux espèces, mais elle joue un rôle crucial dans le maintien de la sélection naturelle, assurant la survie des rennes les plus aptes à la reproduction. Les humains sont également un prédateur majeur, tant par la chasse traditionnelle que par la gestion des populations.

Crédit photo: Alex Kantorovich - Zooinstitutes
Les rennes sont confrontés à un ensemble complexe de menaces, dominé par les changements anthropiques et climatiques. Pour les populations de montagne et de forêt, les aménagements du paysage, tels que les routes et les lignes sismiques liées aux développements forestiers et industriels, entraînent une altération de la végétation et augmentent la vulnérabilité à la prédation. Malgré cette connaissance, les stratégies de gestion demeurent insuffisantes, comme en témoigne le déclin continu du caribou boréal. En Norvège, les infrastructures de transport, les centrales énergétiques et les pôles touristiques fragmentent les populations en faisant obstacle aux migrations. L'exploitation minière locale, source de préoccupations, introduit des problèmes de poussière et des effets cumulatifs. Cependant, l'impact du développement industriel est mieux documenté au niveau individuel que populationnel. Une exception notable concerne la harde du centre de l'Arctique en Alaska, où le développement intensif de champs pétrolifères a affecté la masse corporelle et la survie des faons.
Pour les rennes de la toundra continentale, la chasse non réglementée et la compétition avec les rennes domestiques sont des menaces claires. Bien que le renne soit chassé depuis des millénaires par les peuples autochtones, la technologie moderne a faussé l'effort de chasse, qui n'est plus directement lié à l'abondance des populations, compliquant la détection d'une exploitation non durable. Les réponses de gestion sont fréquemment entravées par la méfiance envers les données scientifiques, le désaccord sur les causes des déclins et les lenteurs institutionnelles à mettre en oeuvre les mesures nécessaires.
Le changement climatique s'accélère dans l'Arctique, générant des effets complexes sur la disponibilité du fourrage, le décalage des périodes de fonte des neiges et de prise/débâcle des glaces. L'un des impacts les plus néfastes est la modification de la fréquence des épisodes de pluie sur neige et de givre, en particulier sur les îles arctiques. Ces événements peuvent entraîner des changements de déplacement majeurs et augmenter la mortalité, notamment chez les faons et les mâles adultes. Un climat plus chaud modifie également l'écologie des parasites : si certains parasites adaptés au froid voient leur développement réduit, les températures accrues changent la répartition des hôtes intermédiaires et des vecteurs, comme les moustiques. Par exemple, des étés plus chauds en Finlande ont intensifié l'activité des moustiques, provoquant des épidémies de Setaria chez les rennes et entraînant de nombreux décès.

Crédit photo: Alex Kantorovich - Zooinstitutes
Le renne est classé dans la catégorie "Vulnérable" (VU) sur la Liste rouge de l'IUCN. Il est également inscrit en Annexe III de la Convention de Berne qui vise à réglementer l'exploitation de cette espèce.
La gestion et la conservation des populations de rennes sont largement encadrées par des plans nationaux, soulignant la vulnérabilité de l'espèce à l'échelle locale. Les évaluations nationales, notamment au Canada (COSEPAC) et en Russie (Livres rouges régionaux), révèlent que les populations de caribous des forêts et des montagnes sont les plus menacées, représentant 84 % des classifications à risque, contre seulement 4 % pour celles de la toundra continentale. Ces classements mènent à des plans de rétablissement ou de gestion spéciale, incluant la protection de l'habitat essentiel.
Contrairement à la majorité des espèces migratrices, le renne n'est pas couvert par la Convention sur les espèces migratrices (CMS), car peu de leurs déplacements traversent des frontières. Néanmoins, une coopération internationale existe pour les deux populations qui migrent entre le Canada et les États-Unis. En Europe, le renne des forêts est classé Quasi menacé en Finlande (Convention de Berne) et fait l'objet d'une surveillance et d'une coopération transfrontalière avec la Russie.
Les systèmes de gestion traditionnels, décrits par Klein (2005), se concentrent sur le suivi démographique et l'ajustement des quotas de chasse. Cependant, les retards dans la mise en oeuvre des mesures, combinés aux avancées technologiques de chasse, accélèrent les déclins. En Norvège, où l'habitat est de plus en plus fragmenté, l'approche évolue vers la gestion du paysage plutôt que la seule gestion des prélèvements.
Malgré l'existence de nombreuses aires protégées, leur efficacité est limitée. La planification de la conservation n'a pas réussi à inverser les causes paysagères du déclin. De plus, les parcs nationaux ne suffisent pas si l'augmentation du tourisme et des loisirs nuit à l'espèce. L'efficacité de ces zones dépend de la mise en place d'un réseau de protection couvrant l'ensemble des aires de répartition annuelles, alors que les zones protégées actuelles se limitent souvent à des aires de répartition saisonnières. Pour les caribous de la toundra, l'accent est mis sur la protection des aires de mise bas, comme le montrent les efforts dans les parcs nationaux canadiens et la réserve de Taimyrski en Russie.

© Kercap - iNaturalist
 CC-BY-NC (Certains droits réservés)
CC-BY-NC (Certains droits réservés)L'histoire taxonomique du renne a été formellement établie par Carl Linnaeus en 1758 dans la dixième édition de son ouvrage fondateur, le Systema Naturae, où il l'a initialement désigné sous le nom de Cervus tarandus, le classant ainsi dans le genre Cervus. Cette désignation initiale reflétait une compréhension rudimentaire des relations phylogénétiques, bien que les rennes fussent reconnus pour leurs bois uniques. C'est plus tard, en 1827, que le genre distinct Rangifer fut créé par le naturaliste britannique Joshua Brookes pour y placer le renne, reconnaissant ainsi les différences morphologiques et comportementales significatives qui le séparent des autres espèces de la famille des Cervidae. Cependant, la taxonomie infra-spécifique, c'est-à-dire la classification des sous-espèces, est historiquement et reste encore aujourd'hui un sujet de débat constant et de révisions fréquentes parmi les mammalogistes et les généticiens.
La grande variabilité du renne sur son vaste aire de répartition holarctique a historiquement mené à la description d'un grand nombre de sous-espèces, bien que la classification moderne basée sur des critères génétiques tende à simplifier cette nomenclature, qui demeure cependant sujette à révision. Les principales divisions se font entre les formes eurasiennes (Rennes) et nord-américaines (Caribous), incluant des formes migratrices de la toundra et des formes sédentaires de la forêt boréale.
* Sous-espèces Nord-Américaines (Caribous)
- Rangifer tarandus caribou (Gmelin, 1788) : Caribou des bois ou Caribou des forêts. Forêts boréales, taïga, et régions montagneuses du Canada (de la Colombie-Britannique au Québec et Labrador) et du Nord-Ouest des États-Unis. Ses populations sont souvent fragmentées.
- Rangifer tarandus groenlandicus (Linnaeus, 1767) : Caribou de la toundra (ou du Barren Ground). Toundra du Nunavut, des Territoires du Nord-Ouest et du Yukon (Canada), ainsi que de l'Ouest du Groenland. Il est connu pour ses vastes migrations.
- Rangifer tarandus pearyi (Allen, 1902) : Caribou de PearyÎles de l'Arctique canadien (archipel Reine-Élisabeth, îles du Nunavut et des Territoires du Nord-Ouest). Il s'agit de la plus petite et de la plus pâle des sous-espèces.
- Rangifer tarandus granti (Allen, 1902) : Caribou de Grant (ou de l'Arctique Occidental). Alaska (États-Unis) et Yukon (Canada). Souvent considéré comme une population migratrice du Rangifer tarandus groenlandicus par certaines classifications.
- Rangifer tarandus dawsoni † (Thompson-Seton, 1900) : Caribou de Dawson. Île Graham, Haida Gwaii (anciennes îles de la Reine-Charlotte), Colombie-Britannique, Canada. Éteint (avant les années 1920).
- Rangifer tarandus eogroenlandicus † (Degerbøl, 1957) : Renne du Groenland oriental. Est du Groenland. Éteint (vers 1900).
* Sous-espèces Eurasiennes (Rennes)
- Rangifer tarandus tarandus (Linnaeus, 1758) : Renne de la toundra eurasienne (ou Renne de montagne norvégien). Toundras et forêts boréales arctiques de l'Eurasie, de la péninsule Scandinave (Norvège, Suède, Finlande) jusqu'au Nord de la Sibérie (Russie). C'est la forme qui comprend la majorité des populations domestiquées.
- Rangifer tarandus fennicus (Lönnberg, 1909) : Renne des forêts de Finlande (ou Renne des forêts eurasiennes). Petites populations sauvages isolées en Finlande et dans la Carélie russe. Il s'agit d'une sous-espèce forestière, moins migratrice et plus grande.
- Rangifer tarandus platyrhynchus (Vrolik, 1829) : Renne du Svalbard (ou Renne du Spitzberg). Archipel du Svalbard (Norvège). C'est la plus petite sous-espèce, très trapue et adaptée à l'environnement insulaire rigoureux.
- Rangifer tarandus phylarchus (Hollister, 1912) : Renne de Sibérie orientale. Régions de taïga et de toundra en Extrême-Orient russe, y compris le Kamchatka et Sakhaline. Souvent reconnu, mais son statut exact est parfois regroupé avec Rangifer tarandus tarandus ou Rangifer tarandus setoni.
Note sur la taxonomie : La reconnaissance de ces sous-espèces est variable. Par exemple, certains scientifiques incluent le Rangifer tarandus setoni (Renne de Sibérie orientale insulaire) ou le Rangifer tarandus montanus (Caribou des montagnes canadiennes), tandis que d'autres les considèrent comme des variations locales des sous-espèces principales (Rangifer tarandus tarandus ou Rangifer tarandus caribou). La liste ci-dessus représente les taxons les plus couramment cités dans la littérature et les bases de données (GBIF, IUCN).

© Manimalworld
 CC-BY-NC-SA (Certains droits réservés)
CC-BY-NC-SA (Certains droits réservés)| Nom commun | Renne |
| Autre nom | Caribou |
| English name | Reindeer |
| Español nombre | Reno Caribú |
| Règne | Animalia |
| Embranchement | Chordata |
| Sous-embranchement | Vertebrata |
| Super-classe | Tetrapoda |
| Classe | Mammalia |
| Sous-classe | Theria |
| Infra-classe | Eutheria |
| Ordre | Artiodactyla |
| Sous-ordre | Ruminantia |
| Famille | Cervidae |
| Sous-famille | Capreolinae |
| Genre | Rangifer |
| Nom binominal | Rangifer tarandus |
| Décrit par | Carl von Linné (Linnaeus) |
| Date | 1758 |
Satut IUCN |  |
* Liens internes
 Liste Rouge IUCN des espèces menacées
Liste Rouge IUCN des espèces menacées
 Mammal Species of the World (MSW)
Mammal Species of the World (MSW)
 Système d'information taxonomique intégré (ITIS)
Système d'information taxonomique intégré (ITIS)
* Liens externes
 Global Biodiversity Information Facility (GBIF)
Global Biodiversity Information Facility (GBIF)
* Bibliographie
 Linnaeus, C. (1758). Systema Naturae per regna tria naturae, secundum classes, ordines, genera, species, cum characteribus, differentiis, synonymis, locis. Editio decima, reformata. Holmiae: Laurentius Salvius.
Linnaeus, C. (1758). Systema Naturae per regna tria naturae, secundum classes, ordines, genera, species, cum characteribus, differentiis, synonymis, locis. Editio decima, reformata. Holmiae: Laurentius Salvius.
 Wilson, D. E., & Reeder, D. M. (Eds.). (2005). Mammal Species of the World: A Taxonomic and Geographic Reference (3rd ed.). The Johns Hopkins University Press. Baltimore.
Wilson, D. E., & Reeder, D. M. (Eds.). (2005). Mammal Species of the World: A Taxonomic and Geographic Reference (3rd ed.). The Johns Hopkins University Press. Baltimore.
 Barth, A. M., Stronen, A. V., & Landa, A. (2018). Phylogeography of the world's northernmost cervid: current knowledge and future perspectives on reindeer (Rangifer tarandus) populations. In S. A. G. H. R. D. M. T. L. B. W. G. B. L. M. E. A. (Eds.), Deer of the World: Ecology, Conservation and Impact. CRC Press.
Barth, A. M., Stronen, A. V., & Landa, A. (2018). Phylogeography of the world's northernmost cervid: current knowledge and future perspectives on reindeer (Rangifer tarandus) populations. In S. A. G. H. R. D. M. T. L. B. W. G. B. L. M. E. A. (Eds.), Deer of the World: Ecology, Conservation and Impact. CRC Press.
 Farnell, R., & Russell, D. (1984). Caribou (Rangifer tarandus) in the Yukon Territory, Canada: distribution, numbers and migration patterns.
Farnell, R., & Russell, D. (1984). Caribou (Rangifer tarandus) in the Yukon Territory, Canada: distribution, numbers and migration patterns.
 Fontana, L. (2023). Le renne (Rangifer tarandus). In Les sociétés de chasseurs de rennes du Paléolithique récent en France. Presses universitaires de Franche-Comté. DOI: 10.4000/books.pufc.50371.
Fontana, L. (2023). Le renne (Rangifer tarandus). In Les sociétés de chasseurs de rennes du Paléolithique récent en France. Presses universitaires de Franche-Comté. DOI: 10.4000/books.pufc.50371.
 Kuntz, D. (2011). Le Renne (Rangifer tarandus) : synthèse sur les taxons et les écotypes.
Kuntz, D. (2011). Le Renne (Rangifer tarandus) : synthèse sur les taxons et les écotypes.
 Muus, B., Salomonsen, F., & Vibe, C. (1990). Grønlands fauna (Fisk, Fugle, Pattedyr). Gyldendalske Boghandel, Nordisk Forlag A/S København.
Muus, B., Salomonsen, F., & Vibe, C. (1990). Grønlands fauna (Fisk, Fugle, Pattedyr). Gyldendalske Boghandel, Nordisk Forlag A/S København.
 Spalding, D. J. (2000). The early history of woodland caribou (Rangifer tarandus caribou) in British-Colombia. Wildlife bulletin (British Columbia. Wildlife Branch), no B-100.
Spalding, D. J. (2000). The early history of woodland caribou (Rangifer tarandus caribou) in British-Colombia. Wildlife bulletin (British Columbia. Wildlife Branch), no B-100.


