Porte-musc nain (Moschus berezovskii)
Le porte-musc nain (Moschus berezovskii) est un petit mammifère artiodactyle appartenant à la famille des Moschidae. Espèce emblématique des forêts montagnardes et subtropicales du sud de la Chine, du nord du Vietnam et du Laos, il constitue l'une des espèces de porte-musc les plus discrètes et les moins étudiées du genre Moschus. Malgré sa discrétion naturelle, cet animal fait face à des menaces sévères liées au braconnage et à la dégradation de son environnement. Classé comme espèce en danger par les instances internationales, il représente un enjeu de conservation majeur pour la biodiversité asiatique, témoignant d'une lignée évolutive ancienne et spécialisée.

© Phil Benstead - iNaturalist
 CC-BY-NC (Certains droits réservés)
CC-BY-NC (Certains droits réservés)Le porte-musc nain est le plus petit représentant du genre Moschus. Les adultes mesurent entre 70 et 100 cm de longueur corporelle, pour une hauteur au garrot comprise entre 43 et 56 cm. Leur masse oscille généralement entre 6 et 9 kg, ce qui les distingue nettement des autres espèces de porte-musc, légèrement plus lourdes. Le pelage est brun foncé à brun rougeâtre sur le dos, avec des flancs plus clairs et une gorge présentant des marques blanches ou jaunâtres caractéristiques sous forme de lignes ou de taches diffuses. Le ventre est généralement plus pâle, tirant sur le crème ou le blanc sale. La tête est petite, avec de grands yeux sombres cerclés d'un anneau clair, des oreilles larges et mobiles couvertes d'un pelage court, et l'absence totale de bois — tant chez les mâles que chez les femelles — ce qui distingue les Moschidae des Cervidae sensu stricto.
Les membres postérieurs sont nettement plus longs que les membres antérieurs, conférant à l'animal une allure légèrement arquée au repos et une grande agilité sur terrain escarpé. Les sabots sont étroits et pointus, adaptés à la progression sur roches et pentes abruptes. Le trait anatomique le plus remarquable du mâle adulte est la présence d'une paire de canines supérieures allongées, dépassant largement les lèvres et pouvant atteindre 6 à 8 cm. Ces défenses sont utilisées lors des combats intra-spécifiques pour l'accès aux femelles. Sur l'abdomen du mâle se trouve une glande musquée prépuciale, en forme de sac cutané, contenant le musc, une sécrétion odorante brun noirâtre solidifiable, utilisée notamment pour le marquage territorial et la communication chimique. Cette glande est absente chez les femelles.

© eMammal - Flickr
 CC-BY-NC-SA (Certains droits réservés)
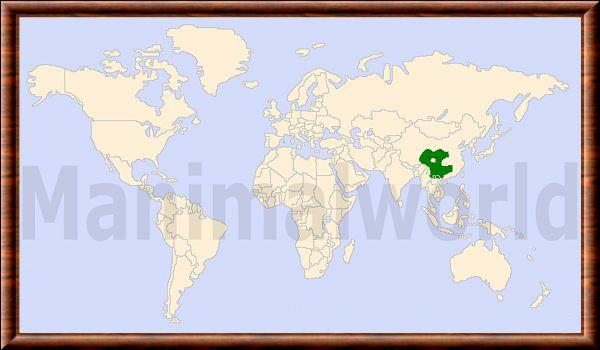
CC-BY-NC-SA (Certains droits réservés)La répartition géographique du porte-musc nain est intrinsèquement liée aux massifs montagneux d'Asie orientale, couvrant une vaste étendue principalement située en Chine. Ce mammifère se rencontre dans une grande diversité de provinces chinoises, notamment au Sichuan, au Yunnan, au Gansu et au Shaanxi, mais ses populations s'étendent également vers l'est et le sud dans le Hubei, le Henan, l'Anhui et le Guangdong. Au-delà des frontières chinoises, l'espèce est présente de manière plus fragmentée dans le nord du Vietnam, particulièrement dans les régions karstiques. Bien que des mentions historiques suggèrent sa présence au Laos, les données actuelles confirment surtout son ancrage dans les zones escarpées de la Chine centrale et méridionale. Son aire de distribution reflète une grande capacité d'adaptation aux reliefs accidentés qui caractérisent ces régions.
En termes d'habitat, le porte-musc nain manifeste une préférence marquée pour les forêts de montagne denses et les zones de broussailles épaisses. Son environnement type se compose de forêts mixtes, de conifères ou de feuillus, offrant un couvert végétal permanent. L'altitude joue un rôle déterminant dans son installation, l'espèce évoluant généralement entre 2 000 et 3 800 mètres d'altitude. Toutefois, cette limite est flexible selon la latitude; dans les zones plus tropicales comme le Vietnam ou le sud de la Chine, il peut être observé dans des forêts de basse montagne dès 400 mètres. La présence d'affleurements rocheux et de pentes abruptes constitue un critère écologique majeur, car ces éléments topographiques servent de refuges naturels et de sites de repos sécurisés. La densité du sous-bois est cruciale pour sa survie, lui permettant de se camoufler efficacement durant ses phases d'inactivité. Malheureusement, la fragmentation des forêts due aux activités humaines restreint de plus en plus la continuité de son habitat originel.
© Manimalworld
 CC-BY-NC-SA (Certains droits réservés)
CC-BY-NC-SA (Certains droits réservés)Le porte-musc nain est un herbivore strictement sélectif se nourrissant préférentiellement de végétaux de haute valeur nutritive plutôt que de grandes quantités de fourrage grossier. Son rumen relativement réduit par rapport aux ruminants de grande taille reflète cette stratégie alimentaire axée sur la qualité plutôt que sur la quantité.
Son régime se compose principalement de lichens arboricoles et rupicoles, de mousses, de pousses tendres, de feuilles de dicotylédones, de fougères, de graminées fines et de fruits tombés au sol. Les lichens jouent un rôle particulièrement important dans son alimentation hivernale, lorsque la neige recouvre les strates herbacées et que les ressources alimentaires se raréfient en altitude. Des champignons hypogés (truffes et autres espèces souterraines) ont également été identifiés dans son régime en certaines saisons, contribuant à ses apports en protéines et en minéraux.

© liuye - iNaturalist
 CC-BY-NC (Certains droits réservés)
CC-BY-NC (Certains droits réservés)La reproduction du porte-musc nain suit un cycle saisonnier marqué, avec une période de rut intervenant généralement entre novembre et janvier dans la majeure partie de son aire de répartition. Durant cette période, les mâles deviennent particulièrement actifs, augmentent leur production de musc et intensifient leur marquage olfactif du territoire. Ils peuvent également émettre des vocalisations discrètes et s'engager dans des confrontations directes avec d'autres mâles, utilisant leurs canines allongées pour infliger des blessures parfois sévères.
Les mâles adoptent une stratégie de défense de ressources plutôt qu'une défense de harem : ils patrouillent et marquent un territoire contenant le domaine vital d'une ou plusieurs femelles, avec lesquelles ils s'accouplent de manière polygyne. La gestation dure environ 185 à 195 jours, soit environ six mois, ce qui place les naissances entre mai et juillet. Les femelles donnent généralement naissance à un ou deux faons, rarement trois. Le faon naît avec un pelage tacheté de blanc, une adaptation cryptique qui lui permet de se dissimuler efficacement dans la végétation dense des sous-bois.
À la naissance, le faon est précoce mais vulnérable : la mère le cache dans des zones de végétation dense et lui rend visite plusieurs fois par jour pour l'allaiter. Le sevrage intervient vers l'âge de 2 à 3 mois. La maturité sexuelle est atteinte vers 18 mois chez la femelle et un peu plus tardivement chez le mâle. La longévité en milieu naturel est estimée à environ 10 à 14 ans, bien que peu de données solides existent pour l'espèce en liberté en raison de sa discrétion. En captivité, des individus ont dépassé 20 ans. Le taux de reproduction relativement faible de l'espèce, combiné à une pression de braconnage importante, rend la dynamique des populations particulièrement fragile.

© eMammal - Flickr
 CC-BY-NC-SA (Certains droits réservés)
CC-BY-NC-SA (Certains droits réservés)Le porte-musc nain est un animal solitaire et territorial, évitant généralement tout contact avec ses congénères en dehors de la période de reproduction. Chaque individu occupe un domaine vital dont la taille varie selon le sexe, la qualité de l'habitat et la disponibilité des ressources alimentaires. Les domaines vitaux des mâles sont en général plus étendus que ceux des femelles et peuvent se superposer partiellement avec ceux de plusieurs femelles, mais rarement avec ceux d'autres mâles.
La communication olfactive joue un rôle central dans l'organisation sociale de l'espèce. Les individus déposent leurs sécrétions sur des rochers, des branches basses et des troncs d'arbres à l'aide de glandes interdigitales, de glandes préputiales (chez le mâle) et par l'urine et les fèces, formant ainsi un réseau de signaux chimiques qui renseigne les congénères sur l'identité, le statut reproducteur et les limites territoriales. Le porte-musc nain est connu pour utiliser des latrines fixes, c'est-à-dire des emplacements régulièrement revisités pour déposer ses déjections, renforçant ainsi les marquages territoriaux.
L'espèce est essentiellement crépusculaire et nocturne, réduisant son activité en pleine journée pour minimiser les risques de prédation. Elle exploite les biotopes rocailleux et les pentes boisées où sa silhouette compacte et sa robe brune la rendent difficile à détecter. En cas de danger, le porte-musc nain fuit à grande vitesse en effectuant des bonds et des changements de direction brusques, exploitant parfaitement les anfractuosités du terrain. Sa capacité à se mouvoir silencieusement dans des sous-bois denses et à rester immobile pendant de longues périodes en fait un animal particulièrement difficile à observer dans la nature.

© Peggy Faucher - iNaturalist
 CC-BY-NC (Certains droits réservés)
CC-BY-NC (Certains droits réservés)En raison de sa petite taille et de son comportement discret, le porte-musc nain est la proie de nombreux prédateurs dans son aire de répartition. Parmi les mammifères carnivores, le léopard (Panthera pardus) - surtout le léopard de Chine du Nord - constituent des menaces importantes dans certaines régions montagnardes. Le loup gris (Canis lupus), présent dans les zones nordiques de l'aire de répartition, représente également un prédateur potentiel, tout comme le dhole (Cuon alpinus), chien sauvage asiatique qui chasse en meutes et peut poursuivre des proies sur de longues distances en terrain accidenté.
Les petits félidés, tels que le chat léopard du Bengale (Prionailurus bengalensis), sont susceptibles de s'en prendre aux jeunes individus ou aux faons encore vulnérables. Parmi les mustélidés, la zibeline (Martes zibellina) et la martre à gorge jaune (Martes flavigula) présentes dans les forêts tempérées et subtropicales de Chine du Sud peuvent occasionnellement chasser de jeunes porte-muscs. Les rapaces de grande taille, comme l'aigle royal (Aquila chrysaetos) et l'aigle de Bonelli (Aquila fasciata), constituent une menace aérienne, notamment pour les faons.

© liuye - iNaturalist
 CC-BY-NC (Certains droits réservés)
CC-BY-NC (Certains droits réservés)La survie du porte-musc nain est gravement compromise par une combinaison de pressions anthropiques et environnementales. La menace la plus directe et historiquement la plus dévastatrice demeure le braconnage intensif. Bien que le musc puisse être extrait d'animaux vivants, les méthodes de piégeage traditionnelles, telles que les collets, ne sont pas sélectives et entraînent souvent la mort de l'animal. Le musc, produit par les glandes du mâle, atteint des prix vertigineux sur le marché noir international, dépassant parfois la valeur de l'or au gramme, ce qui alimente un commerce illégal persistant pour la parfumerie de luxe et la pharmacopée traditionnelle. Outre cette exploitation directe, l'espèce subit une perte d'habitat alarmante. La conversion des forêts en terres agricoles, l'expansion urbaine et le développement d'infrastructures routières fragmentent les populations, isolant des groupes qui deviennent alors vulnérables à la consanguinité et aux extinctions locales. Les perturbations humaines liées à la récolte de bois et de produits forestiers non ligneux stressent également ces animaux naturellement timides, réduisant leur succès reproducteur. Enfin, les changements climatiques récents imposent une pression supplémentaire : les modèles prédictifs pour 2026 suggèrent que le réchauffement global réduit la disponibilité des habitats optimaux à basse altitude, forçant les populations à migrer vers des sommets plus élevés où les ressources alimentaires peuvent être plus limitées et les conditions climatiques plus extrêmes. Cette réduction drastique de son aire de répartition, couplée à un déclin démographique estimé à plus de 50 % au cours des dernières décennies, place le porte-musc nain dans une position critique, particulièrement au Vietnam où l'espèce est désormais considérée comme extrêmement rare.
Le porte-musc nain est considéré comme une espèce menacée. Il est inscrit dans la catégorie "En danger" (EN) sur la Liste rouge de l'IUCN. L'espèce est également inscrite en Annexe II de la CITES.
L'une des stratégies majeures de préservation repose sur le maintien et l'extension des réserves naturelles forestières, visant à sanctuariser les derniers blocs de forêts anciennes essentiels à son cycle de vie. Des efforts particuliers sont déployés pour restaurer la connectivité entre les habitats fragmentés par des corridors biologiques, permettant ainsi les échanges génétiques entre populations isolées. Parallèlement, la Chine a développé un vaste réseau de fermes d'élevage en captivité. Ces structures visent deux objectifs principaux : d'une part, fournir une source légale et contrôlée de musc par extraction non létale pour réduire la pression sur les individus sauvages, et d'autre part, constituer des populations de réserve pour d'éventuels programmes de réintroduction dans la nature. La recherche scientifique actuelle utilise des technologies innovantes comme les pièges photographiques et l'analyse de l'ADN environnemental pour mieux cartographier la présence de l'espèce dans les zones reculées. Des campagnes de sensibilisation auprès des populations locales sont également menées pour lutter contre la pose de collets et promouvoir des alternatives économiques au braconnage. Bien que ces efforts soient significatifs, la pérennité de l'espèce dépendra de l'efficacité de la lutte contre le trafic de musc et de la capacité des gestionnaires à protéger les écosystèmes de haute altitude contre les impacts croissants du développement humain et du changement climatique.

Source: CGTN
L'histoire taxonomique du porte-musc nain est relativement récente et a fait l'objet de nombreuses révisions au cours du XXe siècle. L'espèce a été décrite pour la première fois en 1929 par le zoologiste soviétique Konstantin Konstantinovitch Flerov, sur la base de spécimens collectés dans la province du Sichuan, en Chine centrale. Flerov lui attribua le nom binomial Moschus berezovskii, en hommage au naturaliste russe Mikhail Berezovsky, qui avait collecté des mammifères en Chine à la fin du XIXe siècle pour le compte du Musée zoologique de Saint-Pétersbourg.
Pendant une grande partie du XXe siècle, la taxonomie du genre Moschus fut source de confusion, certains auteurs ne reconnaissant qu'une seule espèce très variable, Moschus moschiferus (porte-musc de Sibérie, et reléguant les autres formes au rang de sous-espèces ou de synonymes. La révision fondamentale de Grubb (1982) fut déterminante pour clarifier la situation : sur la base de critères morphologiques — notamment la coloration du pelage, les proportions crâniennes et les caractères dentaires — il reconnut plusieurs espèces distinctes au sein du genre, dont Moschus berezovskii comme entité valide et autonome.
Des études génétiques ultérieures, notamment celles reposant sur l'analyse de l'ADN mitochondrial et de marqueurs nucléaires, ont globalement confirmé la validité de Moschus berezovskii en tant qu'espèce distincte, tout en précisant ses relations phylogénétiques avec les autres membres du genre. Wang et al. (2003) ainsi que Su et al. (2001) ont mis en évidence que l'espèce forme un clade bien soutenu, génétiquement différencié du porte-musc de Sibérie, du porte-musc de l'Himalaya et du porte-musc noir. Ces résultats ont conduit à un consensus croissant autour d'une classification reconnaissant entre cinq et sept espèces dans le genre Moschus, selon les auteurs.
La position phylogénétique du genre Moschus au sein des ruminants a également fait débat. Longtemps placé parmi les Cervidae en raison de superficies morphologiques partagées, le genre est désormais classé dans la famille monophylétique des Moschidae, que certains phylogénéticiens considèrent comme le groupe frère des Bovidae plutôt que des Cervidae. Cette question reste partiellement ouverte dans la littérature systématique contemporaine.
Les recherches récentes publiées par Liu et al. (2017) et Groves & Grubb (2011) ont en outre mis en lumière la variabilité génétique et phénotypique interne à Moschus berezovskii, suggérant l'existence de plusieurs lignées géographiquement structurées pouvant correspondre à des sous-espèces ou à des unités de gestion distinctes. Ces travaux ont des implications directes pour la conservation, notamment pour éviter le mélange d'individus génétiquement divergents lors des programmes d'élevage en captivité.
La délimitation des sous-espèces reste un sujet débattu dans la littérature taxonomique, en raison de l'insuffisance des données morphologiques et génétiques disponibles pour de nombreuses populations. Plusieurs auteurs ont proposé des subdivisions intra-spécifiques fondées principalement sur des critères géographiques et, dans une moindre mesure, sur des différences de coloration et de mensurations crâniennes.
- Moschus berezovskii berezovskii : est la forme de référence. Elle occupe une vaste zone couvrant le Sichuan, le Gansu et le Shaanxi en Chine. Elle se caractérise par une taille standard et un pelage brun classique.
- Moschus berezovskii bijiangensis : est localisée dans le nord-ouest du Yunnan, habitant des zones de haute altitude où elle a développé des adaptations spécifiques au froid.
- Moschus berezovskii caobangis : vit dans le sud de la Chine et le nord du Vietnam. elle se distingue par une coloration légèrement plus sombre et une taille parfois plus réduite, reflétant son adaptation aux milieux forestiers tropicaux et subtropicaux de basse montagne.
- Moschus berezovskii yanguiensis : est présente dans les régions du Guizhou et du Hunan. Elle ferait l'objet d'une divergence génétique mesurable par rapport aux populations du Sichuan, mais son statut taxonomique formel n'est pas encore stabilisé dans la communauté scientifique et attend une révision systématique complète fondée sur des données génomiques à plus haute résolution.
La validité de ces sous-espèces repose principalement sur des variations morphométriques et des différences de coloration du pelage, bien que les frontières entre leurs aires de répartition puissent parfois se chevaucher. La conservation de chacune de ces lignées est jugée essentielle pour maintenir la diversité génétique globale de l'espèce, car certaines sous-espèces, comme celle du Vietnam, sont particulièrement vulnérables en raison de la petite taille de leurs populations résiduelles.
| Nom commun | Porte-musc nain |
| Nom commun | Porte-musc forestier |
| English name | Dwarf musk deer Forest musk deer |
| Español nombre | Ciervo almizclero enano |
| Règne | Animalia |
| Embranchement | Chordata |
| Sous-embranchement | Vertebrata |
| Super-classe | Tetrapoda |
| Classe | Mammalia |
| Sous-classe | Theria |
| Infra-classe | Eutheria |
| Ordre | Artiodactyla |
| Sous-ordre | Ruminantia |
| Famille | Moschidae |
| Genre | Moschus |
| Nom binominal | Moschus berezovskii |
| Décrit par | Konstantin Konstantinovitch Flerov |
| Date | 1929 |
Satut IUCN |  |
* Liens internes
 Liste Rouge IUCN des espèces menacées
Liste Rouge IUCN des espèces menacées
 Mammal Species of the World (MSW)
Mammal Species of the World (MSW)
 Système d'information taxonomique intégré (ITIS)
Système d'information taxonomique intégré (ITIS)
* Liens externes
 Global Biodiversity Information Facility (GBIF)
Global Biodiversity Information Facility (GBIF)
* Bibliographie
 Flerov, K.K. (1929). A review of the musk-deer of the genus Moschus L. Doklady Akademii Nauk SSSR, série A, pp. 427–430.
Flerov, K.K. (1929). A review of the musk-deer of the genus Moschus L. Doklady Akademii Nauk SSSR, série A, pp. 427–430.
 Dao, V.T. (1969). Sur une nouvelle espèce de chevrotain porte-musc du Nord-Vietnam : Moschus berezovskii caobangis subsp. nov. Zoologicheskii Zhurnal, 48 : 1–12.
Dao, V.T. (1969). Sur une nouvelle espèce de chevrotain porte-musc du Nord-Vietnam : Moschus berezovskii caobangis subsp. nov. Zoologicheskii Zhurnal, 48 : 1–12.
 Grubb, P. (1982). The systematics of Sino-Himalayan musk deer (Moschus), with particular reference to the species described by B.H. Hodgson. Records of the Zoological Survey of India, 80 : 1–18.
Grubb, P. (1982). The systematics of Sino-Himalayan musk deer (Moschus), with particular reference to the species described by B.H. Hodgson. Records of the Zoological Survey of India, 80 : 1–18.
 Su, B., Wang, Y.X., Lan, H., Wang, W. & Zhang, Y. (2001). Phylogenetic study of complete cytochrome b genes in musk deer (Moschus) using museum samples. Molecular Phylogenetics and Evolution, 20(2) : 301–308.
Su, B., Wang, Y.X., Lan, H., Wang, W. & Zhang, Y. (2001). Phylogenetic study of complete cytochrome b genes in musk deer (Moschus) using museum samples. Molecular Phylogenetics and Evolution, 20(2) : 301–308.
 Wang, W., Lan, H., Su, B., Shi, L. & Zhang, Y. (2003). Phylogeography of Yunnan musk deer (Moschus berezovskii) in China based on mitochondrial DNA sequences. Molecular Ecology, 12 : 1873–1880.
Wang, W., Lan, H., Su, B., Shi, L. & Zhang, Y. (2003). Phylogeography of Yunnan musk deer (Moschus berezovskii) in China based on mitochondrial DNA sequences. Molecular Ecology, 12 : 1873–1880.
 Harris, R.B. (2008). Moschus berezovskii. The IUCN Red List of Threatened Species 2008 : e.T13897A4362142. https://dx.doi.org/10.2305/IUCN.UK.2008.RLTS.T13897A4362142.en
Harris, R.B. (2008). Moschus berezovskii. The IUCN Red List of Threatened Species 2008 : e.T13897A4362142. https://dx.doi.org/10.2305/IUCN.UK.2008.RLTS.T13897A4362142.en
 Groves, C. & Grubb, P. (2011). Ungulate Taxonomy. Johns Hopkins University Press, Baltimore, 317 p.
Groves, C. & Grubb, P. (2011). Ungulate Taxonomy. Johns Hopkins University Press, Baltimore, 317 p.
 Liu, Z., Tian, R., Sun, Y., Chen, X., Wu, L., Wang, X. & Li, M. (2017). Genomic evidence for population structure and demographic history of the dwarf musk deer (Moschus berezovskii) in China. Scientific Reports, 7 : 14063.
Liu, Z., Tian, R., Sun, Y., Chen, X., Wu, L., Wang, X. & Li, M. (2017). Genomic evidence for population structure and demographic history of the dwarf musk deer (Moschus berezovskii) in China. Scientific Reports, 7 : 14063.
 Parry-Jones, R. & Wu, J. (2001). Musk Deer Farming as a Conservation Tool in China. TRAFFIC East Asia, Hong Kong.
Parry-Jones, R. & Wu, J. (2001). Musk Deer Farming as a Conservation Tool in China. TRAFFIC East Asia, Hong Kong.
 Green, M.J.B. (1986). The distribution, status and conservation of the Himalayan musk deer (Moschus chrysogaster). Biological Conservation, 35 : 347–375.
Green, M.J.B. (1986). The distribution, status and conservation of the Himalayan musk deer (Moschus chrysogaster). Biological Conservation, 35 : 347–375.
 Wilson, D.E. & Mittermeier, R.A. (eds.) (2011). Handbook of the Mammals of the World. Vol. 2 : Hoofed Mammals. Lynx Edicions, Barcelona, pp. 343–348.
Wilson, D.E. & Mittermeier, R.A. (eds.) (2011). Handbook of the Mammals of the World. Vol. 2 : Hoofed Mammals. Lynx Edicions, Barcelona, pp. 343–348.
 Yang, S. T., et al. (2022). Molecular phylogeny and taxonomy of the genus Moschus in China. Journal of Mammalian Evolution.
Yang, S. T., et al. (2022). Molecular phylogeny and taxonomy of the genus Moschus in China. Journal of Mammalian Evolution.
 Sheng, H. L., & Liu, Z. X. (2007). The Musk Deer in China. Shanghai Scientific and Technical Publishers.
Sheng, H. L., & Liu, Z. X. (2007). The Musk Deer in China. Shanghai Scientific and Technical Publishers.


